天網中國正則工具官方版 一款輕量高效的計算機軟件開發利器
在計算機軟件開發與數據處理領域,正則表達式(Regular Expression)是程序員和數據分析師不可或缺的文本處理工具。它能夠通過簡潔而強大的模式匹配語法,高效地完成字符串的檢索、替換、驗證與提取等復雜操作。原生正則表達式的編寫和測試往往較為晦澀且容易出錯,因此,一款功能直觀、操作便捷的正則工具軟件便成為了眾多開發者的迫切需求。在此背景下,『天網中國正則工具官方版』應運而生,以其官方、純凈、綠色的特性,為用戶帶來了流暢高效的正則表達式應用體驗。
軟件簡介:官方正版,綠色安全
『天網中國正則工具官方版 v1.0綠色版』是一款由天網中國推出的官方正則表達式輔助工具。其“官方版”的身份確保了軟件的來源可靠、功能完整且無惡意捆綁插件,為用戶提供了安全可信的使用基礎。而“綠色版”則意味著軟件無需復雜的安裝過程,下載解壓后即可直接運行,不會在系統中寫入冗余的注冊表信息或產生不必要的系統垃圾,充分體現了其對用戶電腦環境的友好與尊重。目前,用戶可以通過“清風電腦軟件網”等信譽良好的專業軟件下載平臺獲取這款工具,確保了下載渠道的安全與便捷。
核心功能與特色
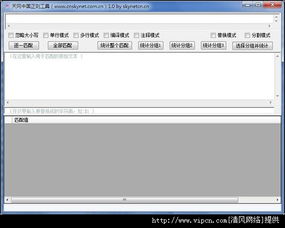
- 直觀的編輯與測試環境:軟件提供了清晰分區的界面,通常包括正則表達式輸入框、待匹配文本輸入區以及匹配結果展示窗口。用戶可以實時編寫正則模式,并立即看到在目標文本中的匹配高亮效果,極大提升了編寫和調試效率。
- 豐富的正則語法支持:工具完整支持主流的正則表達式語法標準,包括各種元字符、字符類、分組、引用、斷言等高級特性,能夠滿足從簡單字符串查找到復雜文本結構解析的各類需求。
- 實用的輔助功能:除了核心的匹配測試,軟件往往還集成替換、生成、常用正則表達式庫等實用功能。用戶可以進行批量替換操作,或從內置庫中快速選取用于匹配郵箱、網址、身份證號等常見格式的正則模板,降低了學習成本。
- 低資源占用與高性能:作為一款綠色輕量級工具,它運行時不占用過多系統內存與CPU資源,即使處理較大的文本文件也能保持流暢的響應速度,是開發者日常工作的得力助手。
在計算機軟件開發中的應用價值
對于計算機軟件開發者而言,正則表達式廣泛應用于日志分析、數據清洗、表單驗證、代碼重構、配置文件解析等場景。『天網中國正則工具官方版』通過可視化的交互方式,使得開發者能夠:
- 快速驗證正則邏輯的正確性,避免因模式錯誤導致程序BUG。
- 加速開發調試進程,將復雜的文本處理邏輯直觀化,縮短開發周期。
- 學習和理解正則表達式,是初學者上手和進階的理想實踐平臺。
獲取與使用建議
建議用戶通過官方指定渠道或如“清風電腦軟件網”這類正規、無病毒的軟件分發網站下載“天網中國正則工具官方版 v1.0綠色版”。下載后,可先進行病毒掃描以確保安全。由于其綠色特性,可以將其存放于U盤或云盤中,實現隨身攜帶、即開即用,在不同工作環境中保持高效的工具流。
###
總而言之,『天網中國正則工具官方版』以其官方背景、綠色免安裝、功能專注且高效的特點,精準地切中了軟件開發者和數據處理人員在文本處理工作中的痛點。它不僅僅是一個工具,更是提升工作效率、保障代碼質量的重要伙伴。在數據驅動的今天,掌握并善用這樣一款利器,無疑能讓您在計算機軟件開發和數據處理的道路上更加游刃有余。
如若轉載,請注明出處:http://www.bwpremierbj.com.cn/product/57.html
更新時間:2026-04-16 13:57:09